

导语:ICU里血糖倏得飙到300,却没给任何糖水?——当术后患者血压尚稳,血糖却先爆表,咱们惯怪肾上腺素。可这条老脚本漏掉了一个荫藏导演:杏仁核。最新小鼠施行告诉你,只须30分钟拘谨,大脑里一群神经元就能把肝糖输出凯旋拉高40%,况且齐全绕过肾上腺。压力性高血糖,蓝本另有专线。
图源:CMT
血糖应激脚本缺页?杏仁核-肝轴跳过肾上腺凯旋拉糖
当机体遭逢环境挟制时,需快速变调能量储备以守旧谛视行为,同期扼制摄食等竞争行为,这一过程依赖下丘脑-垂体-肾上腺(HPA)轴及肾上腺髓质系统调控的激素(如皮质酮、肾上腺素)来变调血糖。过往盘考已证据,血糖升高与“斗殴-逃逸”行为相关,且葡萄糖输注可增强心血管反馈、促进挂念编码,说明应激辅导的糖代谢稳妥具有紧要进化真理。
关联词,当今对调控应激性高血糖及摄食扼制的脑内神经环路机制知之甚少。虽已知杏仁核可合营应激行为稳妥,但对其是否参与代谢变调、具体作用通路及机制仍忙活潜入盘考。经典不雅点合计,应激性血糖变调齐全依赖肾上腺和胰腺激素,而脑区凯旋调控外周代谢的通路尚未被充分挖掘,这一盘考空缺使得学界难以证明为何部分应激性高血糖患者的激素水平无较着相等。
2025年7月,Nature杂志发表了一篇题为“Amygdala–liver signalling orchestrates glycaemic responses to stress”的著作,该盘考初度发现内侧杏仁核(MeA)通过多突触通路连合肝脏,独处于经典激素系统调控应激性血糖,且反复应激会松弛这一环路功能,导致糖尿病样血糖狼藉,为邻策应激与代谢疾病的关联提供了全新视角。

更令药物征战者开心的是,盘考团队用空间转录组在MeA锁定一批高抒发Vglut2且与代谢遗传位点高度疏通的投射神经元,为翌日精确搅扰提供了可靶向的分子。简言之,这份舆图把“心理升糖”写进了可裁剪的神经环路,也为证明“慢性压力→糖尿病”提供了绕过激素的凭证。
化学/光遗传双向考据,轮盘游戏下载同位素示踪算糖账
本盘考是一项基于C57Bl/6小鼠及转基因小鼠(如Vglut2-Cre、Vgat-Cre)的基础施行盘考,旨在明确MeA在应激性糖代谢变调中的作用及神经环路机制,探索反复应激对该环路功能及代谢稳态的影响。
盘考最初通过拘谨应激等竖立急性应激模子,检测小鼠血糖、激素水平及肝脏糖代谢相关基因抒发(如葡萄糖-6-磷酸酶G6pc)。随后接纳化学遗传学(AAV-hSyn-hM3DGq、AAV-hSyn-hM4DGi)、光遗传学(AAV-hSyn-hChR2(H134R))调控MeA神经元及MeA投射至腹内侧下丘脑(VMH)的神经元(MeA^VMH神经元)活性,纪录神经元钙信号(GCaMP8s),不雅察血糖及摄食变化。
通过全身病毒示踪(AAV1-Cre+PRV-GFP)绘图MeA至肝脏的多突触通路,愚弄空间转录组(Xenium)分析MeA^VMH神经元的基因抒发特征。同期,竖立反复应激模子(逐日2次拘谨应激,捏续5天),不雅察MeA神经元活性及血糖变调功能变化;通过要求性敲除MeA^VMH神经元(AAV-FLEX-DTA),评估其对高脂饮食辅导的代谢相等的影响。
主要评价认识包括血糖水平、摄食行为、肝脏糖异生相关基因(G6pc、Foxo1)及卵白(G6Pase、PCK1)抒发、神经环路活性;次要评价认识为血浆激素(皮质酮、肾上腺素、胰岛素、胰高血糖素)水平、肝脏糖原含量、突触连合特征及行为学认识(狂躁样行为)。
30分钟拘谨→MeA神经元放电→肝糖输出增40%,重复应激让环路“熄火”血糖居高不下
急性应激激活MeA^VMH神经元调控血糖
盘考截至裸露,急性拘谨应激可快速升高小鼠血糖(6小时禁食小鼠应激后血糖较对照组权臣升高,澳洲幸运8p<0.001),同期上调肝脏G6pc基因抒发,且这一效应在齐全进食小鼠中不异存在。通过光纤测光发现,拘谨应激、领地cage应激等均能快速激活MeA神经元,且神经元活性升高先于血糖升高(图1),领导MeA神经元可能参与应激性血糖变调。
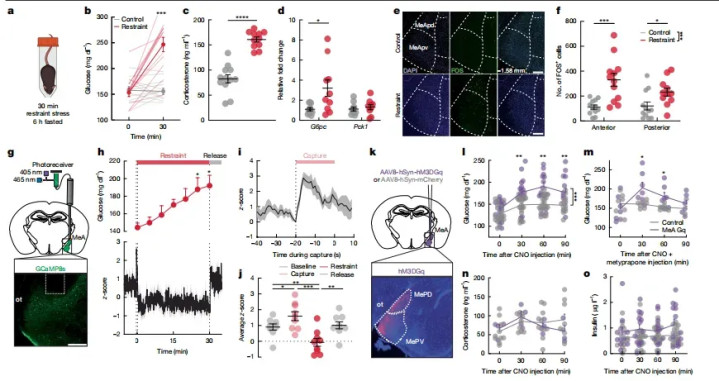
图1 急性拘谨应激激活MeA神经元以变调葡萄糖
注:a.拘谨应激施行经由暗意图;b.无应激(对照)与30min拘谨应激前后血糖水平;c.拘谨应激(红)与无应激(灰)要求下血浆皮质酮变化;d.饱食小鼠资格30min拘谨应激后肝G6pc与Pck1基因抒发的相对倍变;e.对照与30min拘谨小鼠MeA(距前囟−1.58mm)FOS抒发;f.对照与30min拘谨后前部(−1.06至−1.34mm)与后部(−1.34至−2.06mm)MeA FOS+细胞数;g.光纤纪录施行暗意图(上)与GCaMP8s抒发及光纤位置(下);h.拘谨30min技艺MeA GCaMP8s信号z-score(下)与血糖(上)随时辰变化;i.GCaMP8s z-score对皆至捕捉启动时刻;j.基线5min、捕捉30s、拘谨30min、开释5min四阶段平均GCaMP8s z-score;k.MeA化学遗传激活暗意图;l,m.CNO(3mg kg⁻¹腹腔)惩办后6h空心小鼠血糖变化;n,o.CNO惩办后6h空心小鼠血浆皮质酮(n)与胰岛素(o)。
化学激活MeA足以复制升糖,却不碰肾上腺素
CNO激活MeA后15分钟血糖升至峰值(≈250mg/dL vs 基础200mg/dL,p<0.01),而血浆肾上腺素、皮质酮与对照无各异;以致用皮质酮合成扼制剂甲吡酮亦无法阻断升糖(图1)。论断:MeA→升糖通路独处于经典HPA/肾上腺髓质轴。
环路剖解:MeA Vglut2+神经元投射VMH,再经交感神经直抵肝脏
病毒示踪裸露74%的VMH投射神经元为Vglut2+;空间转录组发现这些细胞富集与血糖、T2D相关的基因(Human Genetic Evidence评分>0.5)。光刺激MeA→VMH轴突5分钟,血糖即权臣高于eGFP对照(Δ≈+25mg/dL,图2)。
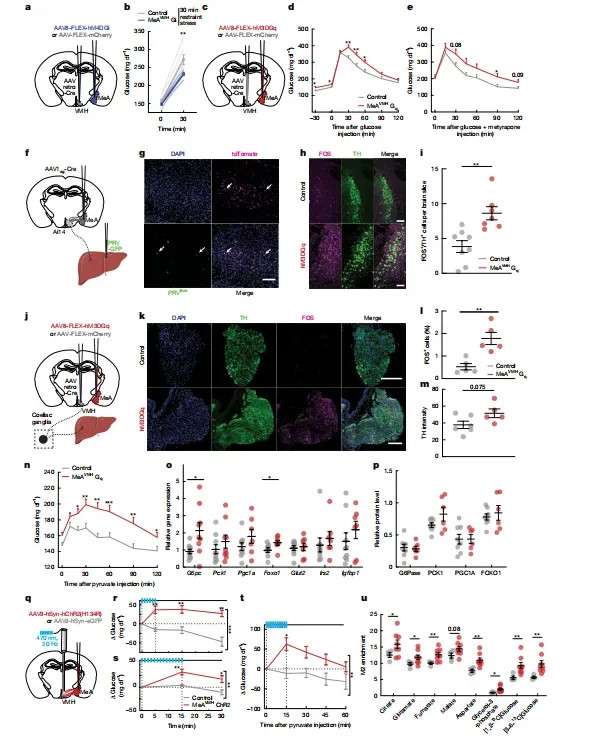
图2 MeA→VMH神经元经交感-肝轴调控血糖
升糖机制:交感驱动肝糖异生,13C丙酮酸掺入增20%
化学激活MeA→VMH后,肝G6pc抒发增1.5倍(p<0.01),腹腔神经节酪氨酸羟化酶(TH)强度升高;赐与[2,3-13C]丙酮酸,M2-柠檬酸、M2-苹果酸等中间居品13C富集度平均擢升20%(图2)。由此,作家指出这一环路升高了血糖。
重复应激让环路“脱敏”,小鼠出现捏续高血糖且高脂饮食下更易糖耐量受损
每12h一次拘谨,第9次时血糖反馈真的消失,MeA-VMH钙信号亦衰减70%以上。更要津的是,愚弄DTA消融30% MeA→VMH神经元后,圭臬饲料即可见体重增6%、立时血糖升15%;换高脂饮食,GTT弧线底下积再增25%,肝β2-肾上腺素受体上调、α2A下调,领导交感失衡(图3)。
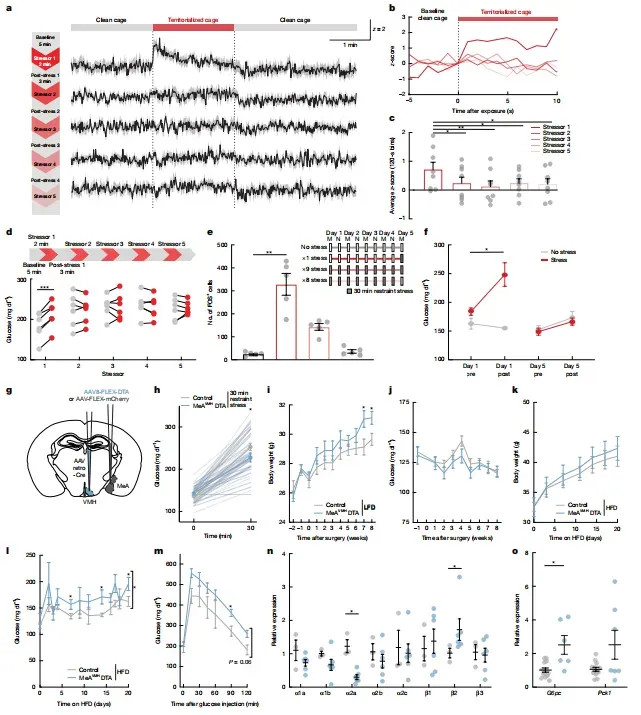
图3 重复应激钝化MeA→VMH环路并诱发代谢相等
转头
本盘考初度绘图出一条不依赖肾上腺的“心理升糖专线”:内侧杏仁核→腹内侧下丘脑→交感神经→肝脏,30分钟内的急性应激即可借说念此轴把肝糖输出拉高四成以上。传统教科书只提肾上腺素、皮质醇,如今必须加上一条神经直连通路,为证明ICU或术后“无激素升糖”提供了回路基础。更临床化的启示在于,重复应激令该清爽脱敏,小鼠随之出现体重增多、糖耐量受损等2型糖尿病前奏。
这意味着恒久思想包袱大的东说念主群,粗略正资格不异的“神经-肝”失控。作家用空间转录组把Vglut2+ MeA神经元标注为可搅扰的“分子邮编”,为翌日征战靶向杏仁核升糖回路的药物或神经调控疗法奠定门路图。简言之,压力与糖尿病之间,不惟有激素,还有一条不错被裁剪的神经高速公路;谁能稳住这条路的信号,谁就可能把应激性高血糖以致2型糖尿病的开始,提前锁死。
参考文件
Carty JRE, Devarakonda K, O'Connor RM, et al. Amygdala-liver signalling orchestrates glycaemic responses to stress. Nature. 2025 Sep 3. DOI: 10.1038/s41586-025-09420-1.
“医学论坛网”发布医学边界盘考遵守妥协读幸运8app,供专科东说念主员科研参考,不算作救援圭臬,使用需根据具体情况评估。
米兰体育官方网站





